.
Condición fitosanitaria: Presente
Grupo de cultivos: Cereales
Especie hospedante: Trigo (Triticum aestivum)
Rango de hospedantes: específico / estrecho
Epidemiología: monocíclica, subaguda.
Etiología: Hongo. Biotrófico
Agente causal: Ustilago tritici (Pers.) Rostr. (Syn Ustilago nuda var. tritici)
Taxonomía: Eukaryota > Fungi > Dikarya > Basidiomycota > Ustilaginomycotina > Ustilaginomycetes > Ustilaginales > Ustilaginaceae > Ustilago
.
Síntomas y signos
Se produce la destrucción total de la flor. Sólo queda el raquis cubierto por una masa pulverulenta de esporas negras. No hay granos y sólo queda el raquis.
.
- Espiga de trigo infectada con carbón volador, causado por Ustilago tritici. La inflorescencia entera, excepto el raquis es reemplazado por masas de teliosporas oscuras. Autor: Thomas Lumpkin/CIMMYT.
- Autor: Clemson University -USDA Cooperative
.
Daños
Puede ser considerada una enfermedad secundaria. Se presenta en la Región Pampeana con bajos valores de incidencia, sin generar daños significativos. Por debajo del 2% de infección las pérdidas no son significativas. En ciertos campos donde el curado de las semillas no es eficiente al no existir una buena cobertura del producto, puede haber mayores pérdidas.
.
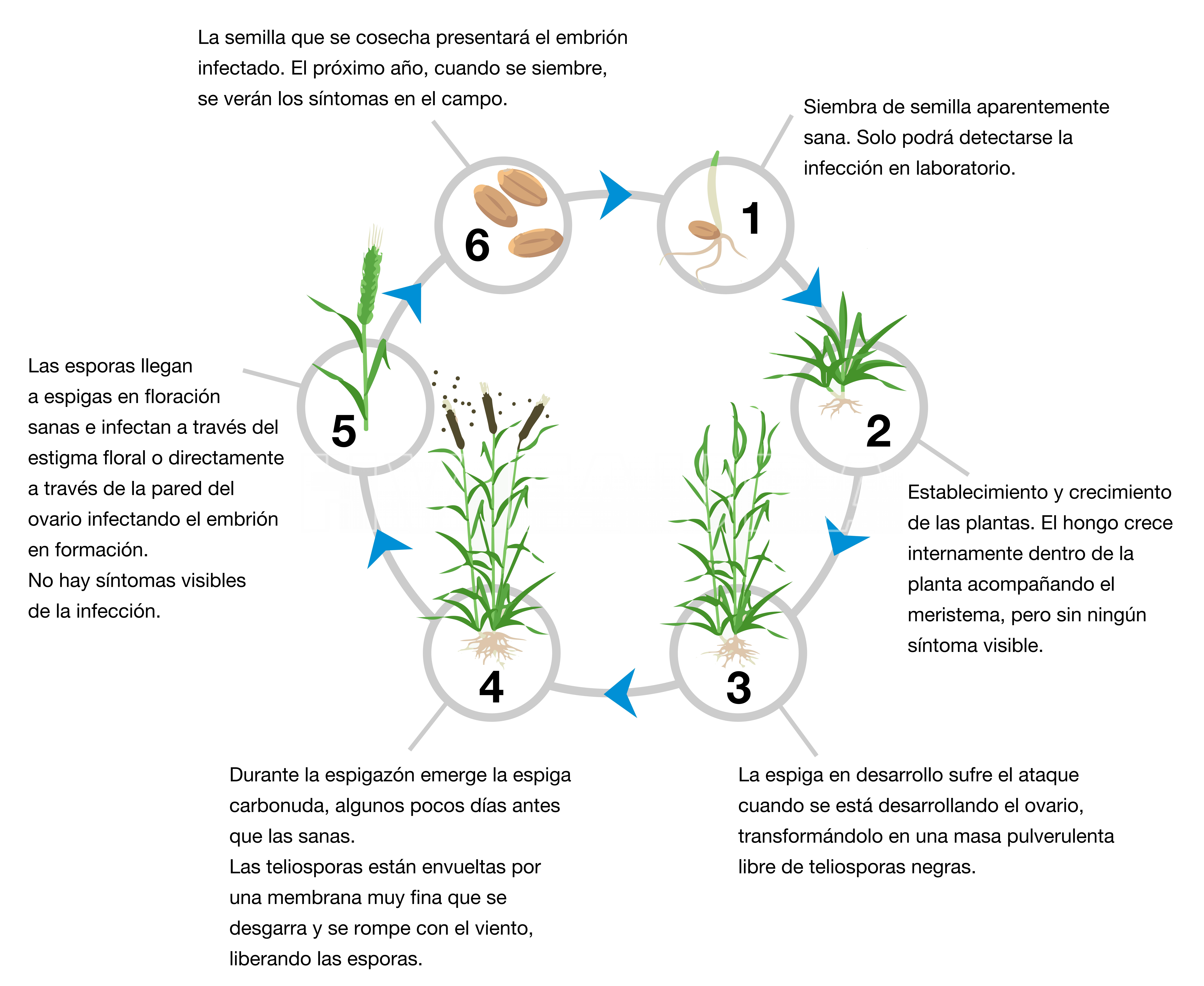
Ciclo de la enfermedad
La infección ocurre durante la floración del trigo. Los granos infectados tienen apariencia normal pero en el interior de embrión se aloja el micelio de hongo en dormición. El patógeno ingresa al ovario, se propaga hacia el embrión y se transmite a la plántula en desarrollo. Cuando se siembra esa semilla en el nuevo ciclo de cultivo, la espiga aparecerá con los síntomas descriptos.
El patógeno infecta a la planta de trigo hospedante durante la floración. Las teliosporas son transportadas por el viento desde las espigas carbonudas hasta los flores de las plantas vecinas y germinan en el ovario. Las hifas infectivas dicarioticas penetran en la pared del ovario y crecen hacia el escutelo y el embrión en desarrollo, donde permanecen latentes hasta la próxima estación de crecimiento, cuando las semillas comienzan a germinar (nuevo cultivo de trigo que se sembrará en el futuro). El hongo coloniza el meristema apical del brote y los primordios de la espiga, dando como resultado el síntoma típico de la espiga carbonuda en el próximo cultivo de trigo (Malik y Batts, 1960a, b).
.
- Ciclo biológico-agronómico del carbón volador de los cereales (Ustilago spp.). Fuente: Carmona y Sautua, 2020.
.
.
Condiciones predisponentes
Alto porcentaje de semillas contaminadas.
.
Manejo
Cultivares resistentes, utilizar semillas sanas o tratadas con funguicidas sistémicos.
.
Cultivares resistentes
A pesar de existir fuentes de resistencia, la mayoría de los cultivares difundidos en Argentina, tienen diverso grado de susceptibilidad.
.
Tratamiento de semillas
Debido al relativamente elevado umbral de daño económico de esta enfermedad (2 % de espigas carbonudas), el esquema de control debería estar dirigido principalmente a los lotes destinados a semilla. Las muestras a sembrar deberían ser analizadas en laboratorios especializados para determinar el nivel de infección especialmente si provienen de campos donde hubo carbón volador. La protección química contra carbón, debería ser llevada a cabo en el caso de contar con una infección en semillas que justifique la aplicación (por ej. 0.5 % de embriones infectados). En el mercado existe una oferta muy amplia de productos.
.
- Autor: Dirceu Gassen
- Carbón volador del trigo. Oro Verde, Paraná (ER). 15-10-2020. Autor: Dra. Norma Formento
- Carbón volador del trigo. Oro Verde, Paraná (ER). 15-10-2020. Autor: Dra. Norma Formento
- Carbón volador del trigo. Oro Verde, Paraná (ER). 15-10-2020. Autor: Dra. Norma Formento
- Carbón volador del trigo. Oro Verde, Paraná (ER). 15-10-2020. Autor: Dra. Norma Formento
- Carbón volador del trigo. Oro Verde, Paraná (ER). 15-10-2020. Autor: Dra. Norma Formento
.
.
.
.
Bibliografía
Alfaro M, Oguiza JA, Ramírez L, Pisabarro AG (2014) Comparative analysis of secretomes in basidiomycete fungi. J Proteomics. 102: 28-43. doi: 10.1016/j.jprot.2014.03.001
Begerow D, Stoll M, Bauer R (2006) A phylogenetic hypothesis of Ustilaginomycotina based on multiple gene analyses and morphological data. Mycologia 98(6): 906-16. doi: 10.1080/15572536.2006.11832620
Kumar S, Knox RE, Singh AK, et al. (2018) High-density genetic mapping of a major QTL for resistance to multiple races of loose smut in a tetraploid wheat cross. PLoS ONE 13(2): e0192261. doi: 10.1371/journal.pone.0192261
Malik MMS, Batts CCV (1960a) The infection of barley by loose smut (Ustilago nuda [Jens.] Rostr.). Transactions of the British Mycological Society 43: 117–125.
Malik MMS, Batts CCV (1960b) The development of loose smut of barley (Ustilago nuda) in the barley plant, with observations on spore formation in nature and in culture. Transaction of the British Mycological Society 43: 126–131.
Ökmen B, Jaeger E, Schilling L, et al. (2022) A conserved enzyme of smut fungi facilitates cell-to-cell extension in the plant bundle sheath. Nat Commun 13: 6003. doi: 10.1038/s41467-022-33815-7
Schuster M, Schweizer G, Kahmann R (2018) Comparative analyses of secreted proteins in plant pathogenic smut fungi and related basidiomycetes. Fungal Genet Biol. 112: 21-30. doi: 10.1016/j.fgb.2016.12.003
Semagn K, Iqbal M, Jarquin D, et al. (2022) Genomic Predictions for Common Bunt, FHB, Stripe Rust, Leaf Rust, and Leaf Spotting Resistance in Spring Wheat. Genes 13(4): 565. doi: 10.3390/genes13040565
Ullmann L, Wibberg D, Busche T, et al. (2022) Seventeen Ustilaginaceae High-Quality Genome Sequences Allow Phylogenomic Analysis and Provide Insights into Secondary Metabolite Synthesis. J Fungi (Basel) 8(3): 269. doi: 10.3390/jof8030269
Wunderle J, Leclerque A, Schaffrath U, et al. (2012) Assessment of the loose smut fungi (Ustilago nuda and U. tritici) in tissues of barley and wheat by fluorescence microscopy and real-time PCR. European Journal of Plant Pathology 133: 865–875. doi: 10.1007/s10658-012-0010-9
Xia W, Yu X, Ye Z (2020) Smut fungal strategies for the successful infection. Microbial Pathogenesis 142: 104039. doi: 10.1016/j.micpath.2020.104039
Yan H, Zhang J, Ma D, Yin J (2019) qPCR and loop mediated isothermal amplification for rapid detection of Ustilago tritici. PeerJ. 30; 7:e7766. doi: 10.7717/peerj.7766
Zuo W, Ökmen B, Depotter JRL, et al. (2019) Molecular Interactions Between Smut Fungi and Their Host Plants. Annual Review of Phytopathology 57: 411-430. doi: 10.1146/annurev-phyto-082718-100139