.
Condición fitosanitaria: Presente
Grupo de cultivos: Hortícolas
Especie hospedante: Papa (Solanum tuberosum)
Etiología: Bacteria. Gram negativa
Agente causal: Pectobacterium carotovorum subsp. carotovorum (Jones, 1901) Waldee, 1945
(previamente Erwinia)
Taxonomía: Bacteria > Proteobacteria > Gammaproteobacteria > Enterobacteriales > Enterobacteriaceae > Pectobacterium > Pectobacterium carotovorum
.
.
Antecedentes e importancia en Argentina
En el cultivo de papa en Argentina, la mayor incidencia de la podredumbre blanda ocurre en poscosecha, principalmente en lotes de papa primicia procedentes de la provincia de Tucumán en la terminación de esta zona de producción (tubérculos inmaduros, gran contenido de agua, altas temperaturas durante la cosecha) y de Villa Dolores en la provincia de Córdoba. Esto se encuentra asociado al movimiento que se realiza de las bolsas de papa cosechada (carga de camiones, descargas con manipuleos poco cuidadosos), por sucesivos golpes que rompen los tubérculos, etc., por lo que el avance de estas podredumbres es en forma violenta.
.
Síntomas
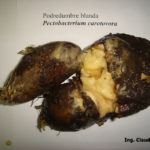
Los síntomas de la pudrición blanda incluyen tejidos blandos, húmedos, podridos, bronceados o de color crema. La pudrición comienza en la superficie del tubérculo y progresa hacia adentro. Los tejidos infectados están claramente delimitados del tejido sano por márgenes de color marrón oscuro o negro. Las manchas necróticas poco profundas en los tubérculos son el resultado de infecciones a través de lenticelas. El tejido podrido suele ser inodoro en las primeras etapas de la descomposición, pero desarrolla un olor fétido cuando los organismos secundarios invaden el tejido infectado. La pudrición blanda también puede infectar tallos y raíces heridos.
Los síntomas podrían confundirse con otras bacterias que causan pudrición, como por ejemplo Dickeya (ver foto de ejemplo en la galería, leer leyendas para no confundir), Bacillus amyloliquefaciens.
.
- Síntomas de Podredumbre blanda de la papa, causada por (Pectobacterium carotovorum subsp. carotovorum. Autor: Ing. Agr. Claudio Baron.
- Síntomas de Podredumbre blanda de la papa, sobre pilas de papa descarte. Autor: Ing. Agr. Claudio Baron.
- Fuente: www.agric.wa.gov.au
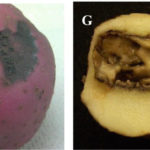
- Izq: Los tubérculos pueden tener lenticelas hinchadas y lesiones hundidas. Der: Las bacterias de la pudrición blanda pueden entrar en el tubérculo a través del estolón y descomponer el centro del tubérculo. Autor: Charkowski AO, Colorado State University
- Tubérculo infectado con Dickeya dianthicola: el tejido podrido es blando, viscoso y empapado de agua; las áreas infectadas a menudo se vuelven marrones o negras alrededor del área podrida al exponerse al aire. Autor: Michigan State University.
.
Patogenicidad
Las pectobacterias de pudrición blanda son patógenos enterobacterianos de amplio rango de hospedantes que causan enfermedades en una variedad de especies de plantas. Las pectobacterias son patógenos necrótrofos agresivos que albergan un gran arsenal de enzimas que degradan la pared celular de las plantas como sus principales determinantes de virulencia. Estas enzimas, junto con factores de virulencia adicionales, se emplean para macerar el tejido del hospedante y promover la muerte de la célula hospedante para proporcionar nutrientes a los patógenos. A diferencia de los (hemi)biotrofos como Pseudomonas, los sistemas de secreción de tipo III (T3SS) y los efectores T3 no parecen ser fundamentales para la patogénesis de las pectobacterias. De hecho, un análisis genómico reciente de varias especies de Pectobacterium, incluido el patógeno emergente Pectobacterium wasabiae (Gardan et al., 2003), ha demostrado que muchas cepas carecen del T3SS completo, así como de los efectores T3. En cambio, este análisis ha indicado la presencia de nuevos determinantes de virulencia. La resistencia genética a pectobacterias de amplio rango de hospedantes es compleja y no parece implicar genes de resistencia individuales. En cambio, la activación de los sistemas de inmunidad innata de las plantas, incluidas las defensas mediadas por SA (ácido salicílico) y JA (ácido jasmónico) / ET (etileno), parece desempeñar un papel central en la atenuación de la virulencia de Pectobacterium. Estas defensas se activan mediante la detección de patrones moleculares asociados a patógenos (PAMP) o el reconocimiento de moléculas propias de la planta modificadas por el patógeno, como los patrones moleculares asociados a daños (DAMP), y dan como resultado una mejora de la inmunidad basal (inmunidad activada por PAMP / DAMP o inmunidad activada por patrones, PTI). En particular, los fragmentos de la pared celular de las plantas liberados por la acción de las enzimas degradantes secretadas por las pectobacterias son actores principales en la inmunidad mejorada o resistencia activada hacia estos patógenos. Más notablemente, las enzimas bacterianas que degradan la pectina liberan fragmentos de oligogalacturónido (OG) reconocidos como DAMP, activan las respuestas inmunitarias innatas. Los avances recientes en la comprensión del reconocimiento y la señalización de OG permiten nuevas posibilidades de screening genético para buscar y hallar mutantes insensibles a OG (Davidsson et al., 2013).
.
Condiciones predisponentes y epidemiología
Las bacterias están presentes en todos los tubérculos y están asociadas con muchos tipos de plantas. En general, las bacterias que producen esta enfermedad suelen estar presentes en las lenticelas de los tubérculos utilizados como semilla. La mayoría de los tubérculos de papa son portadores asintomáticos de una o varias de estas bacterias, que se encuentran protegidas en las lenticelas, pudiendo desarrollar la enfermedad si se dan las condiciones adecuadas para ello. En condiciones ambientales favorables, el inóculo disponible se multiplicará e infectará la planta, penetrando a través de heridas o aberturas naturales. Esa relación cantidad de inóculo-condiciones ambientales determinará la evolución de la infección y, por tanto, los daños producidos. La patogénesis es función de la humedad (la multiplicación de las bacterias se ve favorecida por condiciones de anaerobiosis) y de la temperatura, que favorece a alguna de estas bacterias como organismo predominante. Las infecciones en el campo se ven favorecidas por la alta humedad del suelo y las altas temperaturas. Otros factores incluyen condiciones anaeróbicas, lenticelas agrandadas y la invasión de otros patógenos. Las bacterias entran en lenticelas, grietas de crecimiento o cualquier lesión. Durante y después de la cosecha, la pudrición blanda se ve favorecida por los tubérculos inmaduros, las temperaturas adversas (temperaturas de la pulpa superiores a 22°C durante la cosecha), el daño mecánico y el agua libre en la superficie de los tubérculos.
La bacteria se puede dispersar por el suelo, a través del agua de riego, e infectar nuevas plantas o tubérculos.
Si la planta consigue formar nuevos tubérculos, éstos también estarán infectados, pudiendo producir podredumbres blandas en campo o bien permanecer asintomáticos en el momento de la recolección. Durante su conservación en almacenamiento o en los circuitos de comercialización, la condensación de agua sobre los tubérculos (debida a una mala ventilación) puede generar condiciones de anaerobiosis, favoreciendo la multiplicación de las bacterias y la aparición de pudriciones blandas y malolientes. El mal olor que desprenden los tubérculos infectados se debe a ataques secundarios de otros patógenos que producen ácido butírico y ácido valeriánico.
.
Diagnóstico
Los síntomas inducidos por varias bacterias pueden ser indistinguibles a campo. Por ello, resulta necesaria la realización de análisis en laboratorios especializados para obtener un diagnóstico fiable. El diagnóstico inequívoco del agente causal, Pectobacterium carotovorum subsp. carotovorum, para no confundirlo como otros patógenos como Dickeya and Enterobacter se realiza con técnicas moleculares como la PCR (Ashmawy et al., 2019; Pritchard et al., 2013).
.
Manejo Integrado
Los patógenos que causan estas enfermedades ocurren dondequiera que se cultive papa. La gravedad de la enfermedad depende de las técnicas de manipulación de la papa semilla, la humedad y temperatura del suelo en el momento de la siembra, las condiciones ambientales de cada campaña agrícola particular, el cultivo, la condición fisiológica de la semilla, la densidad de inóculo inicial en el lote de semillas utilizado y las fuentes externas de las bacterias, como el agua de riego y montículos de papa descarte.
* Sembrar papa semilla certificada libre de enfermedades.
* Control Cultural
– Plantar solamente papa semilla de alta calidad.
– Se ha demostrado que las aplicaciones divididas de calcio soluble en agua aplicadas de 112 a 224 kg/ha durante el aumento de volumen reducen la infección y la gravedad de la pudrición blanda.
– Cosechar los tubérculos maduros con baja temperatura de pulpa y cáscaras bien cuajadas, y evitar daños mecánicos.
– Evitar la humedad excesiva del suelo antes de la cosecha para reducir la infección por lenticelas.
– Usar agua limpia para lavar las papas.
– Evitar las películas de agua en las superficies de los tubérculos durante el almacenamiento.
– Las temperaturas de curado y almacenamiento poscosecha pueden ser un componente crítico del manejo de la pudrición blanda. Las recomendaciones de temperatura específicas varían según el nivel de descomposición evidente en el empaque y el destino comercial de las papas (mercado fresco, industria o almacenamiento a largo plazo).
* Los fungicidas no afectan directamente a estos patógenos bacterianos, pero los tratamientos de papa semilla con fungicidas pueden reducir la invasión de otros hongos y, por lo tanto, reducir la infección oportunista por Pectobacterium spp.
* Control biológico
El tratamiento de tubérculos de papa con la cepa Bacillus amyloliquefaciens Ar10 durante 72 h redujo significativamente la gravedad de los síntomas de la enfermedad (reducción del 100 y 85,05% de necrosis profunda / área y pérdida de peso, respectivamente). También se registraron los mismos niveles en la gravedad de los síntomas de la enfermedad después del tratamiento de tubérculos de papa con sobrenadante libre de células durante 1 h. Estos resultados sugieren que la protección contra la pudrición blanda de la papa puede estar relacionada con la producción de glicolípidos por la cepa Ar10 (Azaiez et al., 2018).
.
.
.
.
Bibliografía
Ashmawy NA, El-Bebany AF, Shams AHM, et al. (2020) Identification and differentiation of soft rot and blackleg bacteria from potato using nested and multiplex PCR. Journal of Plant Diseases and Protection 127: 141–153. doi: 10.1007/s41348-019-00257-1
Azaiez S, Slimene IB, Karkouch I, et al. (2018) Biological control of the soft rot bacterium Pectobacterium carotovorum by Bacillus amyloliquefaciens strain Ar10 producing glycolipid-like compounds. Microbiological Research 217:23-33. doi: 10.1016/j.micres.2018.08.013
Charkowski A, Sharma K, Parker ML, et al. (2020) Bacterial Diseases of Potato. In: Campos H., Ortiz O. (eds) The Potato Crop. Springer, Cham. doi: 10.1007/978-3-030-28683-5_10
Czajkowski R, Perombelon MCM, van Veen JA, van der Wolf JM (2011) Control of blackleg and tuber soft rot of potato caused by Pectobacterium and Dickeya species: a review. Plant Pathology 60: 999–1013. doi: 10.1111/j.1365-3059.2011.02470.x
Davidsson PR, Kariola T, Niemi O, Palva ET (2013) Pathogenicity of and plant immunity to soft rot pectobacteria. Front Plant Sci 4:191. doi: 10.3389/fpls.2013.00191
De Boer SH, Rubio I (2004) Blackleg of potato. The Plant Health Instructor. Updated 2016. doi: 10.1094/PHI-I-2004-0712-01
Dees MW, Lysøe E, Rossmann S, et al. (2017) Pectobacterium polaris sp. nov., isolated from potato (Solanum tuberosum). Int J Syst Evol Microbiol 67: 5222–5229. doi: 10.1099/ijsem.0.002448
Dees MW, Lebecka R, Perminow JIS, et al. (2017) Characterization of Dickeya and Pectobacterium strains obtained from diseased potato plants in different climatic conditions of Norway and Poland. Eur J Plant Pathol 148: 839–851. doi: 10.1007/s10658-016-1140-2
Gardan L, Gouy C, Christen R, Samson R (2003) Elevation of three subspecies of Pectobacterium carotovorum to species level: Pectobacterium atrosepticum sp. nov., Pectobacterium betavasculorum sp. nov. and Pectobacterium wasabiae sp. nov. Int. J. Syst. Evol. Microbiol. 53: 381–391. doi: 10.1099/ijs.0.02423-0
Hashemi Tameh M, Primiceri E, Chiriacò MS, et al. (2020) Pectobacterium atrosepticum Biosensor for Monitoring Blackleg and Soft Rot Disease of Potato. Biosensors 10: 64. doi: 10.3390/bios10060064
Joshi JR, Yao L, Charkowski AO, Heuberger AL (2020) Metabolites from Wild Potato Inhibit Virulence Factors of the Soft Rot and Blackleg Pathogen Pectobacterium brasiliense. Molecular Plant-Microbe Interactions. MPMI08200224R. doi: 10.1094/MPMI-08-20-0224-R
Khayi S, Cigna J, Chong TM, et al. (2016) Transfer of the potato plant isolates of Pectobacterium wasabiae to Pectobacterium parmentieri sp. nov. Int J Syst Evol Microbiol 66: 5379–5383. doi: 10.1099/ijsem.0.001524
Li W, Li XB, Suo HC et al. (2017) Soft rot of potatoes caused by Bacillus amyloliquefaciens in Guangdong province, China. Canadian Journal of Plant Pathology 39(4) doi: 10.1080/07060661.2017.1381994
Li X, Fu L, Chen C, et al. (2020) Characteristics and Rapid Diagnosis of Pectobacterium carotovorum ssp. Associated With Bacterial Soft Rot of Vegetables in China. Plant Dis. 104(4): 1158-1166. doi: 10.1094/PDIS-05-19-1033-RE
Lu Q, Yan F, Liu Y, et al. (2021) Comparative Genomic Analyses Reveal Functional Insights Into Key Determinants of the Pathogenesis of Pectobacterium actinidiae in Kiwifruit. Phytopathology. doi: 10.1094/PHYTO-07-20-0287-R
Ma B, Hibbing ME, Kim H-S, et al. (2007) Host range and molecular phylogenies of the soft rot enterobacterial genera Pectobacterium and Dickeya. Phytopathology 97: 1150–1163. doi: 10.1094/PHYTO-97-9-1150
, (2023) Field surveys indicate taxonomically diverse Pectobacterium species inducing soft rot of vegetables and annual crops in Iran. Plant Pathology 00: 1– 12. doi: 10.1111/ppa.13735
Pérombelon MCM, Fox RA, Lowe R (1979) Dispersion of Erwinia carotovora in aerosols produced by the pulverization of potato haulm prior to harvest. J Phytopathol 94: 249–260. doi: 10.1111/j.1439-0434.1979.tb01557.x
Pérombelon MCM, Lowe R, Quinn CE, Ann Sells I (1980) Contamination of pathogen-free seed potato stocks by Erwinia carotovora during multiplication: results of a six-year monitoring study. Potato Res 23:413–425. doi: 10.1007/BF02356257
Pérombelon MCM, Kelman A (1987) Blackleg and other potato diseases caused by soft rot erwinias: proposal for revision of terminology. Plant Disease 71: 283–285.
Pérombelon MCM, Hyman LJ (1989) Survival of soft rot coliforms, Erwinia carotovora subsp. carotovora and E. carotovora subsp. atroseptica in soil in Scotland. J Appl Bacteriol 66: 95–106. doi: 10.1111/j.1365-2672.1989.tb02459.x
Pérombelon MCM (1992) Potato blackleg: epidemiology, host-pathogen interaction and control. Neth J Plant Pathol 98: 135–146. doi: 10.1007/BF01974480
Pritchard L, Humphris S, Saddler GS, et al. (2013) Detection of phytopathogens of the genus Dickeya using a PCR primer prediction pipeline for draft bacterial genome sequences. Plant Pathol 62: 587–596. doi: 10.1111/j.1365-3059.2012.02678.x
Rossmann S, Dees MW, Perminow J, et al. (2018) Soft Rot Enterobacteriaceae Are Carried by a Large Range of Insect Species in Potato Fields. Appl Environ Microbiol. 84(12):e00281-18. doi: 10.1128/AEM.00281-18
Sun H, Jiao WB, Krause K, et al. (2022) Chromosome-scale and haplotype-resolved genome assembly of a tetraploid potato cultivar. Nat Genet. doi: 10.1038/s41588-022-01015-0
, , , et al. (2021) Characterization of Pectobacterium brasiliense strains from potato and vegetables in Israel. Plant Pathology 70: 2179– 2187. doi: 10.1111/ppa.13454
van der Wolf JM, Nijhuis EH, Kowalewska MJ, et al. (2014) Dickeya solani sp. nov., a pectinolytic plant pathogenic bacterium isolated from potato (Solanum tuberosum). Int J Syst Evol Microbiol 64: 768–774. doi: 10.1099/ijs.0.052944-0
van der Wolf JM, Haan EG, Kastelein P, et al. (2017) Virulence of Pectobacterium carotovorum subsp. brasiliense on potato compared with that of other Pectobacterium and Dickeya species under climatic conditions prevailing in the Netherlands. Plant Pathol 66: 571–583. doi: 10.1111/ppa.12600
, , , et al. (2020) Pectobacterium atrosepticum KDPG aldolase, Eda, participates in the Entner–Doudoroff pathway and independently inhibits expression of virulence determinants. Molecular Plant Pathology 22: 271– 283. https://doi.org/10.1111/mpp.13025
Zhang JX, Lin BR, Shen HF, et al. (2012) First Report of Bacterial Soft Rot of Potato Caused by Pectobacterium carotovorum subsp. carotovorum in Guangdong Province of China. Plant Disease 96(12): 1819. doi: 10.1094/PDIS-07-12-0620-PDN