.
Condición fitosanitaria: Presente
Grupo de cultivos: Cereales
Especie hospedante: Trigo (Triticum aestivum)
Rango de hospedantes: en discusión
Etiología: Hongo. Hemibiotrófico
Agente causal: Pyricularia oryzae pathotype Triticum (PoT) (teleomorfo = Magnaporthe oryzae B.C. Couch, 2002)
Taxonomía: Fungi > Ascomycota > Pezizomycotina > Sordariomycetes > Magnaporthales > Magnaporthaceae > Pyricularia
.
(*) Hay controversia en cuanto al nombre del agente causal. Ceresini et al. (2019) propusieron el nombre Pyricularia graminis-tritici (Pygt). Sin embargo, Valent et al. (2019) argumentaron que ese nombre no sería correcto, y elaboran un resumen de «la abrumadora evidencia que respalda la designación alternativa, reconocida internacionalmente, de Pyricularia oryzae (sin. Magnaporthe oryzae; Zhang et al., 2016) como una sola especie dividida en linajes adaptados al hospedante con rango de hospedantes primarios limitado.»
El tizón por Pyricularia en trigo es causada por un linaje del hongo ascomycota P. oryzae que está adaptado para causar epidemias en hospedantes del género Triticum (Cruz y Valent, 2017; Islam et al., 2016; Urashima et al., 1993).
Un análisis genómico en profundidad reciente de una gran colección mundial de aislados de P. oryzae de diferentes plantas hospedantes ha preservado a P. oryzae como una sola especie (Gladieux et al., 2018). Estos investigadores analizaron la estructura filogenética dentro de la especie P. oryzae, basándose en secuencias del genoma completo de 76 cepas recolectadas de 12 géneros de hospedantes distintos, más cinco cepas de especies relacionadas de Pyricularia. Esta clasificación es consistente con investigaciones previas sobre formas del hongo adaptadas al hospedante y la última delimitación de especies de P. oryzae (Klaubauf et al., 2014).
.
.
Antecedentes
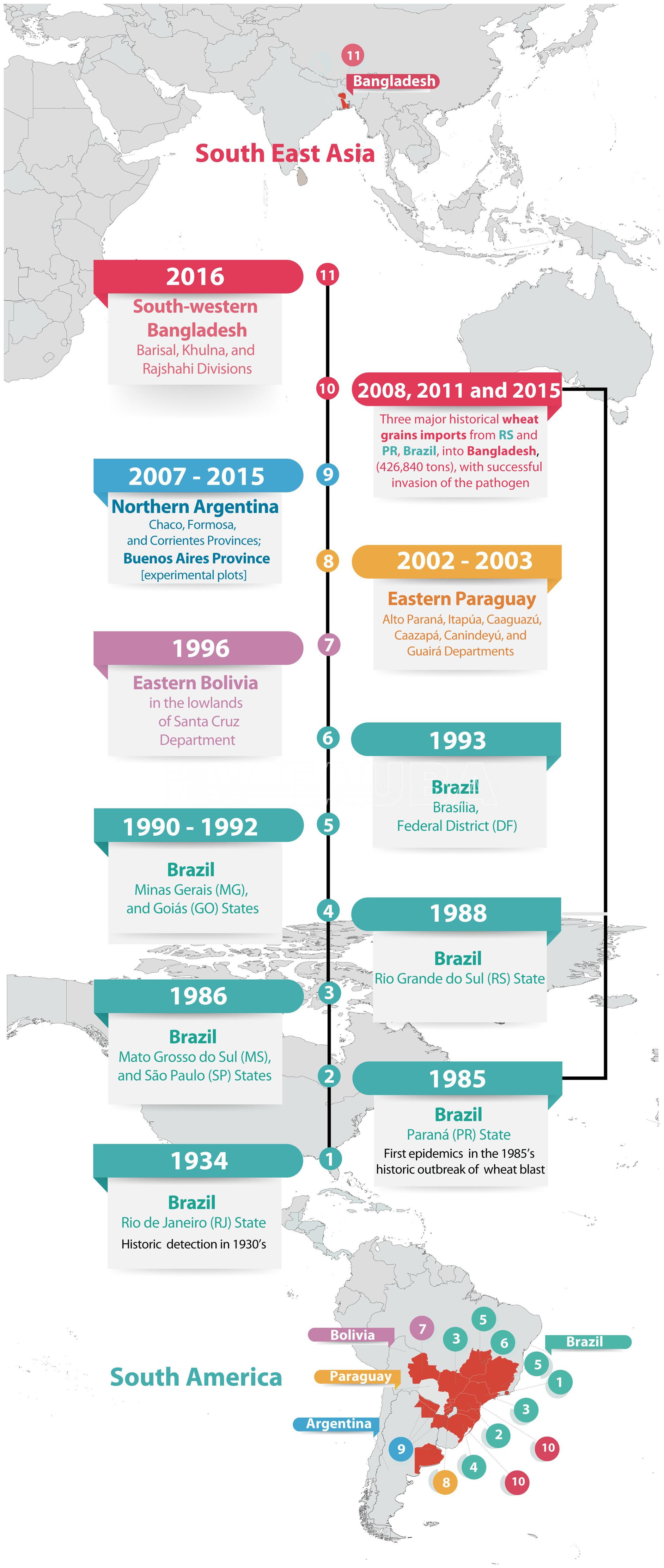
La enfermedad se descubrió por primera vez en el estado de Paraná, Brasil en 1985 (Igarashi et al., 1986); se encontró en los estados vecinos de São Paulo y Mato Grosso do Sul en 1986 (Goulart et al., 1990), seguido de Rio Grande do Sul en 1987 (Igarashi, 1991). Desde entonces, se ha convertido en una enfermedad importante en el centro y sur de Brasil, y ahora está bien establecida en América del Sur. La enfermedad no estaba muy extendida en Brasil antes de la epidemia de 1985 (Igarashi, 1991; Igarashi et al., 1986), aunque una descripción previa de 1936 (Puttemans, 1936) sugiere que el tizón del trigo puede haber estado ya presente en el estado de Río de Janeiro.
.
- Cronología de los acontecimientos de la propagación del tizón por Pyricularia en trigo, desde su aparición en América del Sur hasta su invasión al sudeste asiático. Las regiones de trigo confirmadas con la enfermedad se resaltan en rojo. Autor: Ceresini et al., 2019.
.
Síntomas y signos
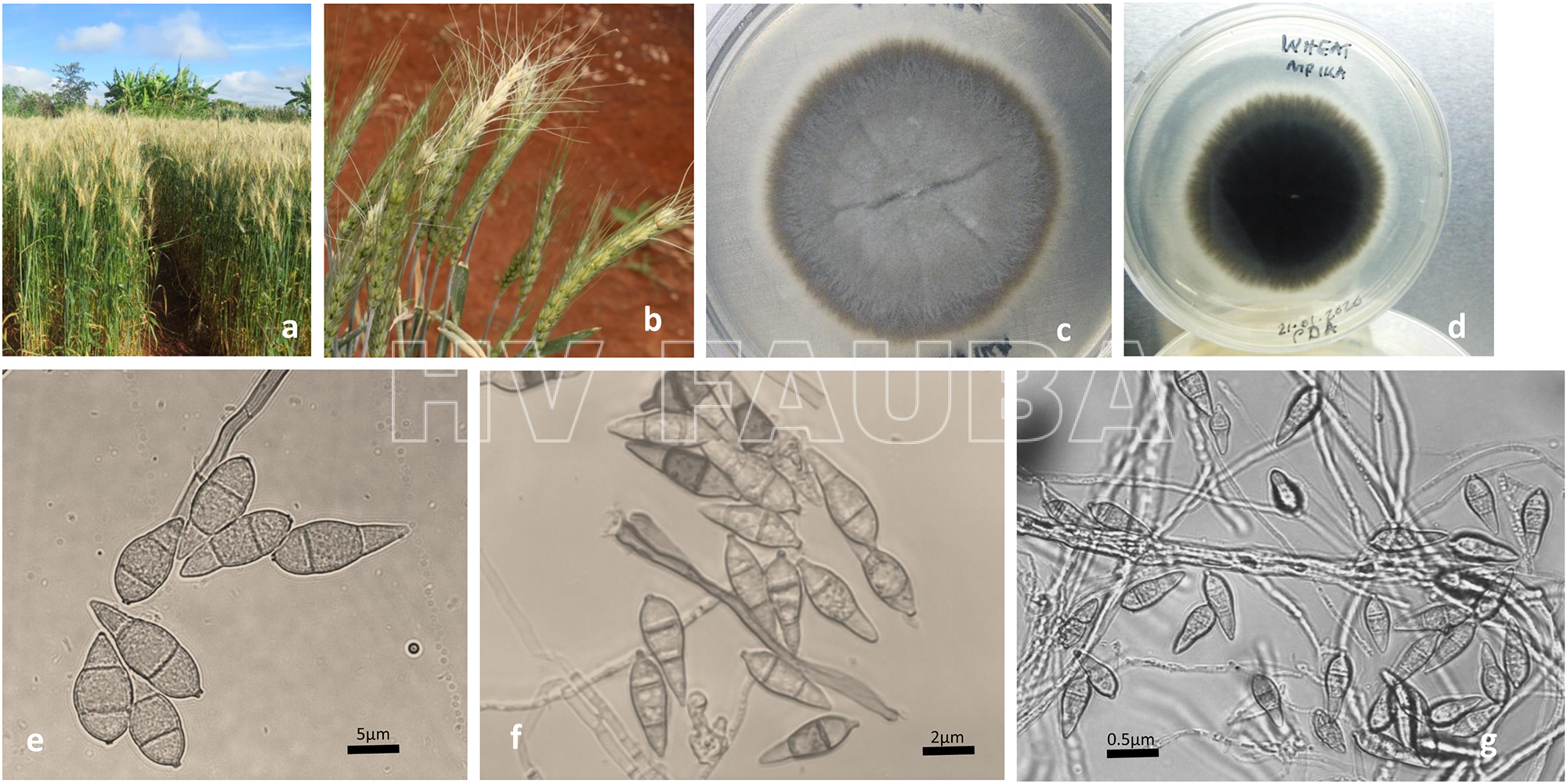
El síntoma más visible a campo es el blanqueamiento o blanquecimiento de la espiga. Este síntoma particular es similar al producido por la Fusariosis, espiga blanca o golpe blanco del trigo causado por Fusarium graminearum (Maciel et al., 2013). Las aristas infectadas muestran decoloración marrón a blanquecina, mientras que las glumas infectadas muestran lesiones elípticas con márgenes de color marrón rojizo a gris oscuro. En las hojas, las lesiones macroscópicas iniciales son gris-verde, con mancha de agua (water soaked). Las lesiones tienen centros grises durante la esporulación, y centros blancos a bronceados después de la esporulación. Las lesiones maduras a menudo tienen un margen marrón oscuro a marrón rojizo que detiene la expansión de la lesión, y también suelen tener halos cloróticos amarillos. Las lesiones individuales generalmente tienen forma de mancha ocular o eye-spot shaped, a veces elípticas, pero se unen en plántulas infectadas de forma moderada a severa, lo que a veces puede resultar en la muerte total de la planta (Rios et al., 2013).
.
- (A) Espigas de trigo “blanqueadas”, naturalmente infectadas con Pyricularia. (B) Síntomas del tizón del trigo por Pyricularia en plantas inoculadas en invernadero. (C) Cultivo de Magnaporthe oryzae patotipo Triticum (MoT) del aislado WS4. Se pueden observar micelios grises en el fondo y micelios aéreos blancos. (D) El color del micelio en el reverso del mismo aislado se ve oscuro. (E), (F) y (G). Esporas de MoT aisladas de plantas inoculadas en el invernadero. Las esporas se identificaron utilizando un microscopio digital Motic BA310. Autor: Tembo et al 2020.
.
Daños e importancia económica
Esta enfermedad ha sido importante en Sudamérica desde la década de 1980, en países como Brasil y Paraguay. En Argentina fue reportada en trigo en la provincia de Formosa en el 2007 (Cabrera y Gutiérrez, 2007), en la provincia de Buenos Aires en 2015 (Perelló et al., 2015), y en cebada en la provincia de Corrientes en el 2012 (Gutiérrez y Cúndom, 2015). Si bien esta enfermedad aún no es de importancia epidemiológica para nuestro país, su prevalencia está aumentando. Esta enfermedad fue reportada por primera vez en el estado de Paraná , Brasil en 1985, y desde entonces su intensidad e importancia ha crecido hasta el día de hoy, dispersándose a través de todas las regiones trigueras en Brasil (Igarashi et al., 1986; Anjos et al., 1996; Kohli et al., 2011). En Brasil se han reportado daños de 40% y hasta 100% de rendimiento (Goulart et al., 2007; Maciel, 2011). Incluso se ha detectado resistencia a fungicidas inhibidores de la quinona externa o estrobilurinas (Castroagudín et al., 2015). En el 2016, la enfermedad fue reportada por primera vez fuera de Sudamérica en Bangladesh (Malaker et al., 2016). De acuerdo con un análisis de patogenómica se confirmó que el hongo se dispersó muy probablemente desde América del Sur hasta Bangladesh (Islam et al., 2016). La semilla está implicada en la dispersión a largas distancias (Goulart y Paiva 1990).
Los granos de espiguillas infectadas en cultivares altamente susceptibles a menudo son pequeños, marchitos y deformados, con bajo peso (Goulart et al. 2007).
.
Condiciones predisponentes
La combinación de altas temperaturas, lluvia excesiva, mojado foliar prolongado y frecuente favorecen la aparición epidémica de esta enfermedad (Goulart et al., 2007). El período crítico requiere temperatura óptima que oscila entre 25 y 30°C con 25 y 40 horas de mojado de espiguillas (Cardoso et al., 2008). Estos dos factores por sí solos pueden favorecer la intensidad de Pyricularia o brusone del trigo.
Fernandes et al. (2017) desarrollaron un modelo predictivo de epidemias de Pyricularia o brusone del trigo basado en datos climáticos. La infección diaria exitosa (INF) durante un día conducente para la infección (DFI) estuvo condicionado a las interacciones entre la temperatura y la humedad relativa, y al inóculo potencial (IP) y la nube de esporas (SPOR).
.
Ciclo de la enfermedad y epidemiología
El patógeno sobrevive en semillas y rastrojo (Gomes et al., 2017). Asimismo, Pygt puede infectar un amplio rango de hospedantes gramíneas, tales como Hordeae, Festuceae, Avenae, Chlorideae, Agrosteae y Paniceae (Castroagudín et al., 2017). Colectivamente, el complejo de especies que causan la enfermedad pueden infectar más de 50 especies de gramíneas, incluyendo arroz (Oryza sativa L.), trigo (Triticum aestivum L.), mijo africano (Eleusine coracana), mijo italiano (cola de zorra) (Setaria italica), Ryegrass perenne y anual (Lolium species), avena (Avena sativa), cebada (Hordeum vulgare L.) y crabgrass (Digitaria sanguinalis (L.) Scop) (Cruz y Valent, 2017).
Los análisis filogenéticos indican que Pygt es una especie patógena con un elevado grado de diversidad genética, con un amplio rango de hospedantes, que abarca muchas gramíneas nativas o introducidas en Brasil. Sin embargo, aún no se han encontrado peritecios en los campos de trigo que presentan la enfermedad, y aún no está claro dónde y cuándo se produce la etapa sexual (Castroagudín et al., 2017). Bajo condiciones de laboratorio se observó el desarrollo de peritecios madures sobre Phalaris canariensis. Se hipotetiza que Pygt pasa la mayor parte de su ciclo de vida colonizando especies de pastos vecinos o que invaden los campos de trigo afectados por la enfermedad. Además, se postula que la recombinación sexual tiene lugar principal o exclusivamente en estos otros hospedantes poáceos, generando la mayor parte de la diversidad genética observada en las poblaciones de Pygt que infectan al trigo (Castroagudín et al., 2017).
Los conidios del patógeno puede dispersarse a cortas y largas distancias a través del viento.
.
Manejo Integrado de la enfermedad:
* Resistencia genética. Al momento se han identificaron algunos genes de resistencia como por ejemplo los genes Rmg8 y Rmg7 (Anh et al., 2017). Sin embargo, la única fuente de resistencia que hasta ahora ha dado resultados satisfactorios es aquella aportada en cultivares de trigo que portan un gran segmento del brazo cromosómico 2NS de Aegilops ventricosa / Triticum ventricosum translocado a la parte distal del brazo cromosómico 2NS del trigo común (T. aestivum L.), comunmente denominada «translocación 2NS» (2NS Translocation) (Cruz et al., 2016). Esta región cromosómica fue introducida en los materiales de trigo de Paraguay y Brasil a traves de una linea del CIMMYT llamada Milan. Esta translocación esta presente en las variedades Canindé 1 y CD 116 (Braun et al., 2017).
* Rotación con hospedantes no gramíneas.
* En Brasil, Paraguay y Bolivia, retrasar la fecha de siembra ha reducido significativamente las pérdidas de rendimiento (Coelho et al., 2016). El objetivo es evitar coincidir la espigazón del trigo durante períodos de altas temperaturas, altas precipitaciones y alta humedad relativa.
.
- 01 Síntomas de Pyricularia o brusone en trigo observados a campo. Espigas con la parte inferior verde y la superior blanca (Capitán Miranda, Itapúa, Paraguay, 2015). Autor: Ing. Agr. Alice Chávez
- 02 Punto de infección en el ráquis de la espiga, el color gris oscuro a negro es por el crecimiento micelial y esporulación del hongo. Autor: Ing. Agr. Alice Chávez
- 03 Punto de infección en el ráquis de la espiga, el color gris oscuro a negro es por el crecimiento micelial y esporulación del hongo. Autor: Ing. Agr. Alice Chávez
- 02 Espiga de trigo con síntoma típico de Pyricularia o brusone. Autor: Ing. Agr. Alice Chávez
- 05 Conidios de Pyricularia, aislados a partir de síntomas de brusone en trigo.
.
.
.
Bibliografía
Anh VL, Inoue Y, Asuke S, et al. (2017) Rmg8 and Rmg7, wheat genes for resistance to the wheat blast fungus, recognize the same avirulence gene AVR-Rmg8. Molecular Plant Pathology (in press). doi: 10.1111/mpp.12609
Anjos JRND, Silva DBD, Charchar MJD, Rodrigues GC (1996) Ocurrence of blast fungus (Pyricularia grisea) on wheat and rye in the savanna region of Central Brazil. Pesquisa Agropecuária Brasileira 31: 79-82.
Arora S, Steed A, Goddard R, et al. (2022) A wheat kinase and immune receptor form the host-specificity barrier against the blast fungus. bioRxiv 2022.01.27.477927; doi: 10.1101/2022.01.27.477927
Ascari JP, Cazón LI, Rahnama M, et al. (2023) Pyricularia Populations are Mostly Host-Specialized with Limited Reciprocal Cross-Infection Between Wheat and Endemic Grasses in Minas Gerais, Brazil. bioRxiv 2023.01.20.524950; doi: 10.1101/2023.01.20.524950
Aucique-Pérez CE, Resende RS, Martins AO, et al. (2020) How do wheat plants cope with Pyricularia oryzae infection? A physiological and metabolic approach. Planta 252(2): 24. doi: 10.1007/s00425-020-03428-9
Braun H, Singh P, Khan SH, Govindan V (2017) Liberan la primera variedad de trigo biofortificado resistente al quemado o brusone del trigo en Bangladesh. CIMMYT
Cabezas SRM, Silva GS (2015) Pyricularia oryzae em cultivos de cevada na região de Corrientes (Argentina). Summa Phytopathologica 41(4): 318-320. doi: 10.1590/0100-5405/2063
Cabrera MG, Gutiérrez S (2007) Primer registro de Pyricularia grisea en cultivos de trigo del NE de Argentina. Jornada de Actualización en Enfermedades de Trigo. IFSC Press, Lavallol, Buenos Aires.
Cardoso CDA, Reis EM, Moreira EN (2008) Development of a warning system for wheat blast caused by Pyricularia grisea. Summa Phytopathologica 34:216–221. doi: 10.1590/S0100-54052008000300002
Castroagudín VL, Ceresini PC, Oliveira SC, et al. (2015) Resistance to QoI fungicides is widespread in Brazilian populations of the wheat blast pathogen Magnaporthe oryzae. Phytopathology 104: 284-294. doi: 10.1094/PHYTO-06-14-0184-R. PMID: 25226525.
Castroagudín VL, Moreira SI, Pereira DAS, et al. (2016) Pyricularia graminis-tritici, a new Pyricularia species causing wheat blast. Persoonia 37: 199–216. doi: 10.3767/003158516X692149
Castroagudín VL, Danelli ALD, Moreira SI, et al. (2017) The wheat blast pathogen Pyricularia graminis-tritici has complex origins and a disease cycle spanning multiple grass hosts. BioRxiv, online Oct. 16, 2017; doi: 10.1101/203455
Ceresini PC, Castroagudín VL, Rodrigues FÁ, et al. (2019), Wheat blast: from its origins in South America to its emergence as a global threat. Molecular Plant Pathology, 20: 155-172. doi: 10.1111/mpp.12747
Chanclud E, Win J, Malone J, et al. (2017) Genome sequences of candidate wheat blast biocontrol bacteria. figshare. doi: 10.6084/m9.figshare.5558641.v1
Chávez A, Cazal C, Kohli M (2017) Diferencia en la reacción a Pyricularia oryzae de materiales de trigo en los estadios vegetativo y reproductivo. Investigación Agraria 19(1): 56-63. doi: 10.18004/investig.agrar.2017.junio.56-63
Chávez AR, Tellez LC, Cazal-Martinez CC, et al. (2022) Further progress on wheat blast epidemiology: Identification of novel alternate hosts of Magnaporthe oryzae Triticum pathotype in Paraguay. Eur J Plant Pathol. doi: 10.1007/s10658-022-02567-x
Coelho MDO, Torres GM, Cecon PR, Santana FM (2016) Sowing date reduces the incidence of wheat blast disease. Pesquisa Agropecuária Brasileira 51: 631–637. doi: 10.1590/S0100-204X2016000500025
Consolo VF, Milazzo J, Adreit H, et al. (2017) Caracterización de cepas de «Magnaporthe oryzae» de distintos hospedantes y virulencia en arroz y trigo. E.E.A. Concepción del Uruguay, C.R. Entre Ríos. LINK
Cruz CD, Kiyuna J, Bockus WW, et al. (2015) Magnaporthe oryzae conidia on basal wheat leaves as a potential source of wheat blast inoculum. Plant Pathology 64: 1491-1498. doi: 10.1111/ppa.12414
Cruz CD, Peterson GL, Bockus WW, et al. (2016) The 2NS Translocation from Aegilops ventricosa Confers Resistance to the Triticum Pathotype of Magnaporthe oryzae. Crop Science 56: 990-1000. doi: 10.2135/cropsci2015.07.0410
Cruz MFA, Rios JA, Araujo L, et al. (2016) Infection process of Pyricularia oryzae on the leaves of wheat seedlings. Tropical Plant Pathology 41(2): 123–127. doi: 10.1007/s40858-016-0068-6
Cruz CD, Magarey D, Christie DN, et al. (2016) Climate Suitability for Magnaporthe oryzae Triticum Pathotype in the United States. Plant Disease 100(10): 1979-1987. doi: 10.1094/PDIS-09-15-1006-RE
Cruz CD, Valent B (2017) Wheat blast disease: danger on the move. Tropical Plant Pathology 42(3): 210–222. doi: 10.1007/s40858-017-0159-z
De la Concepcion JC, Franceschetti M, Maqbool A, et al. (2018) Polymorphic residues in rice NLRs expand binding and response to effectors of the blast pathogen. Nature Plantsvolume 4: 576–585. doi: 10.1038/s41477-018-0194-x
Debona D, Rios JA, Nascimento KJ, et al. (2016) Influence of magnesium on physiological responses of wheat infected by Pyricularia oryzae. Plant Pathology 65: 114-123. doi: 10.1111/ppa.12390
Dong Y, Li Y, Zhao M, et al. (2015) Global Genome and Transcriptome Analyses of Magnaporthe oryzae Epidemic Isolate 98-06 Uncover Novel Effectors and Pathogenicity-Related Genes, Revealing Gene Gain and Lose Dynamics in Genome Evolution. PLoS Pathog 11(4): e1004801. doi: 10.1371/journal.ppat.1004801
Duan G, Bao J, Chen X, et al. (2021) Large-Scale Genome Scanning within Exonic Regions Revealed the Contributions of Selective Sweep Prone Genes to Host Divergence and Adaptation in Magnaporthe oryzae Species Complex. Microorganisms 9(3): 562. doi: 10.3390/microorganisms9030562
Dutta S, Surovy MZ, Gupta DR, et al. (2018) Genomic analyses reveal that biocontrol of wheat blast by Bacillus spp. may be linked with production of antimicrobial compounds and induced systemic resistance in host plants. figshare doi: 10.6084/m9.figshare.5852661.v1
Farman ML, Ascari JP, Rahnama M, et al. (2024) A Reevaluation of Phylogenomic Data Reveals that Current Understanding in Wheat Blast Population Biology and Epidemiology Is Obfuscated by Oversights in Population Sampling. Phytopathology 114(1): 220-225. doi: 10.1094/PHYTO-01-23-0025-R
Feng W, Yin Z, Wu H, et al. (2021) Balancing of the mitotic exit network and cell wall integrity signaling governs the development and pathogenicity in Magnaporthe oryzae. PLoS Pathog 17(1): e1009080. doi: 10.1371/journal.ppat.1009080
Fernandes JMC, Nicolau M, Pavan W, et al. (2017) A weather-based model for predicting early season inoculum build-up and spike infection by the wheat blast pathogen. Tropical Plant Pathology 42(3): 230–237. doi: 10.1007/s40858-017-0164-2
Fernandez J, Orth K (2018) Rise of a Cereal Killer: The Biology of Magnaporthe oryzae Biotrophic Growth. Trends in Microbiology (In press). doi: 10.1016/j.tim.2017.12.007
, , , et al (2023) Multiscale temporal and spatiotemporal analysis of wheat blast infection-like dynamics using vertical plant stratification, regression and Markov chain approaches. Plant Pathology 72: 1570–1584. doi: 10.1111/ppa.13789
Gladieux P, Condon B, Ravel S, et al. (2018) Gene flow between divergent cereal- and grass-specific lineages of the rice blast fungus Magnaporthe oryzae. mBio 9:e01219-17. doi: 10.1128/mBio.01219-17
Gomes DP, Rocha VS, Pereira OL, de Souza MA (2017) Damage of wheat blast on the productivity and quality of seeds as a function of the initial inoculum in the field. Journal of Seed Science 39(1): 66-74 (online). doi: 10.1590/2317-1545v39n1172688
Goulart ACP, Paiva FA (1990) Transmission of Pyricularia oryzae by wheat Triticum aestivum seeds. Fitopatol Brasileira 15: 359–362.
Goulart ACP, Sousa PG, Urashima AS (2007) Damages in wheat caused by infection of Pyricularia grisea. Summa Phytopathologica 33(4): 358-363. doi: 10.1590/S0100-54052007000400007
Gupta DR, Khanom S, Rohman MM, et al. (2021) Hydrogen peroxide detoxifying enzymes show different activity patterns in host and non-host plant interactions with Magnaporthe oryzae Triticum pathotype. Physiol Mol Biol Plants. 27(9): 2127-2139. doi: 10.1007/s12298-021-01057-4
Howard RJ, Valent B (1996) Breaking and entering: host penetration by the fungal rice blast pathogen Magnaporthe grisea. Annu Rev Microbiol. 50: 491-512. doi: 10.1146/annurev.micro.50.1.491
Igarashi S, Utiamada CM, Igarashi LC, et al. (1986) Pyricularia em trigo. Ocorrência de Pyricularia sp. no estado do Paraná. Fitopatol Brasileira 11: 351-352.
Islam MT, Croll D, Gladieux P, et al. (2016) Emergence of wheat blast in Bangladesh was caused by a South American lineage of Magnaporthe oryzae. BMC Biology 14:11. doi: 10.1186/s12915-016-0309-7
Kaundal R, Kapoor AS, Raghava GP (2006) Machine learning techniques in disease forecasting: a case study on rice blast prediction. BMC Bioinformatics 7: 485. doi: 10.1186/1471-2105-7-485
, , , (2014) Resolving the polyphyletic nature of Pyricularia (Pyriculariaceae). Stud. Mycol. 79: 85–120. doi: 10.1016/j.simyco.2014.09.004
Kohli MM, Mehta YR, Guzman E, et al. (2011) Pyricularia blast – a threat to wheat cultivation. Czech Journal of Genetics and Plant Breeding 47: S130-S4. LINK
Kunova A, Pizzatti C, Cortesi P (2013) Impact of tricyclazole and azoxystrobin on growth, sporulation and secondary infection of the rice blast fungus, Magnaporthe oryzae. Pest Management Science 69: 278-284. doi: 10.1002/ps.3386
Kunova A, Pizzatti C, Bonaldi M, Cortesi P (2014) Sensitivity of nonexposed and exposed populations of Magnaporthe oryzae from rice to tricyclazole and azoxystrobin. Plant Disease 98: 512-518. doi: 10.1094/PDIS-04-13-0432-RE
Latorre SM, Were VM, Foster AJ, et al. (2023) Genomic surveillance uncovers a pandemic clonal lineage of the wheat blast fungus. PLoS Biol 21(4): e3002052. doi: 10.1371/journal.pbio.3002052
Liu S, Lin G, Ramachandran SR, et al. (2022) Rapid mini-chromosome divergence among fungal isolates causing wheat blast outbreaks in Bangladesh and Zambia. bioRxiv 2022.06.18.496690; doi: 10.1101/2022.06.18.496690
Liu S, Lin G, Ramachandran SR, et al. (2023) Rapid mini-chromosome divergence among fungal isolates causing wheat blast outbreaks in Bangladesh and Zambia. New Phytol. doi: 10.1111/nph.19402
Luo J, Zhang N (2021) The Rice Blast Fungus and Allied Species: A Monograph of the Fungal Order Magnaporthales. LINK
Maciel JLN (2011) Magnaporthe oryzae, the blast pathogen: current status and options for its control. Plant Sci Rev.: 233-240. doi: 10.1079/PAVSNNR20116050.
Maciel JLN, Danelli ALD, Boaretto C, Forcelini CA (2013) Diagrammatic scale for the assessment of blast on wheat spikes. Summa phytopathologica 39(3): 162-166. doi: 10.1590/S0100-54052013000300003
Maidment JHR, Franceschetti M, Maqbool A, et al. (2021) Multiple variants of the fungal effector AVR-Pik bind the HMA domain of the rice protein OsHIPP19, providing a foundation to engineer plant defence. J Biol Chem.: 100371. doi: 10.1016/j.jbc.2021.100371
Malaker PK, Barma NCD, Tiwari TP, et al. (2016) First report of wheat blast caused by Magnaporthe oryzae pathotype triticum in Bangladesh. Plant Disease 100(11): 2330–2330. doi: 10.1094/PDIS-05-16-0666-PDN
Martínez SI, Sanabria A, Fleitas MC, et al. (2019) Wheat blast: Aggressiveness of isolates of Pyricularia oryzae and effect on grain quality. Journal of King Saud University – Science 31: 150-157. doi: 10.1016/j.jksus.2018.05.003
Martinez S, Wegner A, Bohnert S, et al. (2021) Tracing seed to seeding transmission of the wheat blast pathogen Magnaporthe oryzae pathotype Triticum. Plant Pathology 70: 1562-1571. doi: 10.1111/ppa.13400
Motoyama T (2020) Secondary Metabolites of the Rice Blast Fungus Pyricularia oryzae: Biosynthesis and Biological Function. Int J Mol Sci. 21(22): 8698. doi: 10.3390/ijms21228698
Murmu S, Archak S (2023) In-silico study of protein-protein interactions in wheat blast using docking and molecular dynamics simulation approach. J Biomol Struct Dyn. 25:1-11. doi: 10.1080/07391102.2023.2228907
Nguyen QT, Ueda K, Tamura T, et al. (2018) Antifungal activity of a novel compound purified from the culture filtrate of Biscogniauxia sp. O821 against the rice blast fungus Magnaporthe oryzae. Journal of General Plant Pathology: 1–6. doi: 10.1007/s10327-018-0767-6
O’Hara T, Steed A, Goddard R, et al. (2023) The wheat powdery mildew resistance gene Pm4 also confers resistance to wheat blast. bioRxiv 2023.09.26.559489. doi: 10.1101/2023.09.26.559489
Oliveira TB, Aucique-Pérez CE, Rodrigues FA (2019) Foliar application of silicon decreases wheat blast symptoms without impairing photosynthesis. Bragantia 78: 423-431. doi: 10.1590/1678-4499.20180379
Perelló A, Martinez I, Molina M (2015) First Report of Virulence and Effects of Magnaporthe oryzae Isolates Causing Wheat Blast in Argentina. Plant Disease 99(8): 1177. doi: 10.1094/PDIS-11-14-1182-PDN
, , , et al. (2021) Widespread distribution of resistance to triazole fungicides in Brazilian populations of the wheat blast pathogen. Plant Pathol 70: 436– 448. doi: 10.1111/ppa.13288
Prahl KC, Klink H, Hasler M, et al. (2022) Can Decision Support Systems Help Improve the Sustainable Use of Fungicides in Wheat? Sustainability 14(23): 15599. doi: 10.3390/su142315599
Rabby SMF, Chakraborty M, Gupta DR, et al. (2022) Bonactin and Feigrisolide C Inhibit Magnaporthe oryzae Triticum Fungus and Control Wheat Blast Disease. Plants (Basel) 11(16): 2108. doi: 10.3390/plants11162108
Rios JA, Debona D, Duarte HSS, Rodrigues FA (2013) Development and validation of a standard area diagram set to assess blast severity on wheat leaves. European Journal of Plant Pathology 136: 603–611. doi: 10.1007/s10658-013-0191-x
Rios JA, Rios VS, Aucique-Pérez CE, et al. (2017) Alteration of photosynthetic performance and source–sink relationships in wheat plants infected by Pyricularia oryzae. Plant Pathology 66: 1496-1507. doi: 10.1111/ppa.12693
Rodrigues FÁ, Rios JA, Debona D, et al. (2017) Pyricularia oryzae-wheat interaction: physiological changes and disease management using mineral nutrition and fungicides. Trop. plant pathol. 42: 223–229. doi: 10.1007/s40858-017-0130-z
Sakulkoo W, Osés-Ruiz M, Oliveira Garcia E, et al. (2018) A single fungal MAP kinase controls plant cell-to-cell invasion by the rice blast fungus. Science 359, Issue 6382: 1399-1403. doi: 10.1126/science.aaq0892
Sharma R (2017) Wheat blast research: Status and imperatives. African Journal of Agricultural Research 12(6): 377-381. doi: 10.5897/AJAR2016.11860
Shi NN, Ruan HC, Liu XZ, et al. (2018) Virulence structure of Magnaporthe oryzae populations from Fujian Province, China. Canadian Journal of Plant Pathology. doi: 10.1080/07060661.2018.1504821
Silva ET, Rios JA, Araujo MUP, et al. (2019) Defence responses in flag leaves and spikes of common wheat Triticum aestivum cultivars with contrasting levels of basal resistance to blast caused by Pyricularia oryzae. Plant Pathology 68: 645-658. doi: 10.1111/ppa.12979
Surovy MZ, Gupta DR, Chanclud E, et al. (2017) Plant probiotic bacteria suppress wheat blast fungus Magnaporthe oryzae Triticum pathotype. figshare. doi: 10.6084/m9.figshare.5549278.v1
Tang W, Gao C, Wang J, et al. (2018) Disruption of actin motor function due to MoMyo5 mutation impairs host penetration and pathogenicity in Magnaporthe oryzae. Molecular Plant Pathology 19: 689–699. doi: 10.1111/mpp.12554
Tembo B, Mulenga RM, Sichilima S, et al. (2020) Detection and characterization of fungus (Magnaporthe oryzae pathotype Triticum) causing wheat blast disease on rain-fed grown wheat (Triticum aestivum L.) in Zambia. PLoS ONE 15(9): e0238724. doi: 10.1371/journal.pone.0238724
, (1993) Host range, mating type and fertility of Pyricularia grisea from wheat in Brazil. Plant Dis. 77, 1211–1216. doi: 10.1094/PD-77-1211
Urashima AS, Alves AF, Silva FN, et al. (2017) Host range, mating type and population structure of Magnaporthe sp. of a single barley field in São Paulo state, Brazil. Journal of Phytopathology 165: 414–424. doi: 10.1111/jph.12575
Valent B, Farman M, Tosa Y, et al. (2019), Pyricularia graminis-tritici is not the correct species name for the wheat blast fungus: response to Ceresini et al. (MPP 20:2). Molecular Plant Pathology 20: 173-179. doi: 10.1111/mpp.12778
Valent B, Cruppe G, Stack JP, et al. (2021) Recovery Plan for Wheat Blast Caused by Magnaporthe oryzae Pathotype Triticum. Plant Health Progress 22: 182-212. doi: 10.1094/PHP-11-20-0101-RP
Vales M, Anzoátegui T, Huallpa B, et al. (2018) Review on resistance to wheat blast disease (Magnaporthe oryzae Triticum) from the breeder point-of-view: use of the experience on resistance to rice blast disease. Euphytica 214: 1. doi: 10.1007/s10681-017-2087-x
Vicentini SNC, Casado PS, de Carvalho G, et al. (2022) Monitoring of Brazilian wheat blast field populations reveals resistance to QoI, DMI, and SDHI fungicides. Plant Pathology 71: 304– 321. doi: 10.1111/ppa.13470
Vicentini SNC, Moreira SI, da Silva AG, et al. (2022) Efflux Pumps and Multidrug-Resistance in Pyricularia oryzae Triticum Lineage. Agronomy 12(9): 2068. doi: 10.3390/agronomy12092068
Vicentini SNC, Hawkins NJ, King KM, et al. (2023) Aerobiology of the Wheat Blast Pathogen: Inoculum Monitoring and Detection of Fungicide Resistance Alleles. Agronomy 13(5): 1238. doi: 10.3390/agronomy13051238
Wang S, Asuke S, Vy TTP, et al. (2018) A new resistance gene in combination with Rmg8 confers strong resistance against Triticum isolates of Pyricularia oryzae in a common wheat landrace. Phytopathology (accepted). doi: 10.1094/PHYTO-12-17-0400-R
Wang Z, Xia Y, Lin S, et al. (2018) Osa‐miR164a targets OsNAC60 and negatively regulates rice immunity against the blast fungus Magnaporthe oryzae. The Plant Journal 95: 584-597. doi: 10.1111/tpj.13972
Wang S, Wang J, Zhang Z, et al. (2021) The risk of wheat blast in rice-wheat-co-planting regions in China: MoO strains of Pyricularia oryzae cause typical symptom and host reaction on both wheat leaves and spikes. Phytopathology. doi: 10.1094/PHYTO-10-20-0470-R
Xiang Z, Okada D, Asuke S, et al. (2022) Novel insights into host specificity of Pyricularia oryzae and Pyricularia grisea in the infection of gramineous plant roots. Mol Plant Pathol. 23(11): 1658-1670. doi: 10.1111/mpp.13259
, , , et al. (2020) A review on South Asian wheat blast: The present status and future perspective. Plant Pathology 69: 1618– 1629. doi: 10.1111/ppa.13250
Zhang N, Luo J, Rossman AY, et al. (2016) Generic names in Magnaporthales. IMA Fungus 7: 155–159. doi: 10.5598/imafungus.2016.07.01.09
Zhang W, Huang J, Cook DE (2021) Histone modification dynamics at H3K27 are associated with altered transcription of in planta induced genes in Magnaporthe oryzae. PLoS Genet 17(2): e1009376. doi: 10.1371/journal.pgen.1009376
Zhong X, Yang J, Shi Y, et al. (2018) The DnaJ protein OsDjA6 negatively regulates rice innate immunity to the blast fungus Magnaporthe oryzae. Molecular Plant Pathology 19: 607–614. doi: 10.1111/mpp.12546
, , , et al. (2021) The COMPASS‐like complex modulates fungal development and pathogenesis by regulating H3K4me3‐mediated targeted gene expression in Magnaporthe oryzae. Molecular Plant Pathology 00: 1– 18. doi: 10.1111/mpp.13035