.
Condición fitosanitaria: Presente
Grupo de cultivos: Frutales
Especie hospedante: Numerosas especies arbóreas correspondientes a frutales, forestales y ornamentales.
Rango de hospedantes: amplio, no específico
Epidemiología: monocíclica, crónica.
Etiología: Hongo. Necrotrófico
Agente causal: Diversos hongos Basidiomycetes del subphylum Agaricomycotina, que comprenden géneros como Ganoderma, Polyporus, Fomes, Phellinus, Armillaria, entre otros.
Taxonomía: Fungi > Basidiomycota > Agaricomycotina > Agaricomycetes
Antecedentes: Comprende un grupo muy amplio de hongos que forman basidios típicos, sin tabiques.
.
Los basidiomycetes causantes de caries de los árboles presentan características morfológicas particulares. Por ejemplo, un basidiocarpo o basidioma es el esporocarpo de un hongo basidiomycota, que consiste en una estructura multicelular sobre la que se dispone el himenio productor de basidiosporas. Los basidiocarpos son característicos de los Agaricomycetes, Dacrymycetes y algunos Tremellomycetes y Atractiellomycetes, al contrario de lo que sucede con el resto de los basidiomicetos que no tienen estas estructuras (Ingold, 1992).
Muchas especies de basidiomycetes presentan fíbulas, también llamadas conexión en fíbula (unión en fíbula), en abrazadera o clamp (del inglés, clamp connection). La fíbula es una estructura que se produce entre dos células binucleadas adyacentes de una misma hifa; y contribuye a que durante la mitosis de una célula con dos núcleos (A y B), las copias de ambos núcleos (A’ y B’) se mantengan en la nueva célula.
.
- Colonia de Armillaria. Autor: Dr. Matt Kasson
.
.
.
Subphylum AGAROMYCOTINA
Comprende un grupo muy amplio de hongos que forman basidios típicos, sin tabiques. Dentro de los fitopatógenos pertenecen a esta subclase los hongos causantes de las Caries de los árboles. Estas enfermedades se caracterizan por la podredumbre de la madera, la cual pierde densidad y adquiere diversas coloraciones según los procesos enzimáticos involucrados en la desintegración:
- Podredumbres castañas o pardas: Los hongos que las causan producen enzimas que degradan la celulosa y hemicelulosa, pero no afectan la lignina. Generalmente atacan árboles de madera blanda.
- Podredumbres blancas: Los hongos responsables de estas enfermedades producen, además de las mencionadas anteriormente, enzimas lignolíticas. Los árboles de madera dura, generalmente resistentes a los anteriores, son atacados por estos hongos.
Los basidios generalmente se forman en basidiocarpos, fructificaciones macroscópicas de tamaño y colores variados, en algunos casos muy vistosas (ej. géneros Ganoderma, Laetiporus).
.
Algunos órdenes de importancia agronómica son:
.
AGARICALES (Hongos de sombrero o Setas)
Este orden comprende una gran variedad de hongos, muchos de ellos benéficos, ectomicorríticos, descomponedores de madera y algunas especies comestibles.
Los basidiocarpos son los típicos “hongos de sombrero” con un pie, el estípite, y los basidios tapizando las laminillas que conforman el sombrero o píleo.
Géneros (ejemplos):
Armillaria spp. A. mellea provoca la pudrición de raíces en un amplio rango de especies frutales y forestales. El hongo desarrolla abundante micelio entre el leño y la corteza, desintegrando el floema y el cambium. Además forma rizomorfas que facilitan el avance, llegando a ocupar un solo ejemplar un radio de varias hectáreas, y la supervivencia del hongo, ya que una vez muerto el hospedante pueden sobrevivir años en forma saprofítica y seguir fructificando. Los basidiocarpos se forman típicamente en la periferia de las colonias circulares en anillos y se los denomina vulgarmente “cono de brujas”.
Pleurotus spp
.
POLYPORALES (ex APHYLLOPHORALES) (Hongos en estante)
Los basidios son producidos en basidiocarpos sobre un himenio (capa fértil) que tapiza pequeños poros o tubos. Comprenden muchas especies descomponedoras de la madera en árboles vivos y en madera cortada.
Géneros (ejemplos):
Ganoderma spp: causan podredumbres basales y de raíces en coníferas, maderas duras, palmeras y árboles tropicales.
Laetiporus spp (ex Polyporus): causan podredumbres en árboles vivos y también en madera cortada.
Trametes spp Fr., 1835: causan podredumbres blancas.
.
HYMENOCHAETALES
Géneros (ejemplos):
Phellinus spp: causan podredumbres de raíces en la mayoría de las coníferas y muchas especies de madera dura, y también en madera cortada.
.
.
- Laetiporus cincinnatus. Autor: Alan Windham
- Trametes versicolor. Autor: Bob McIntosh
.
Síntomas
El hongo penetra hasta el interior de la rama o tronco a través de heridas, podas, rotura de ramas, etc., ante la exposición del duramen al exterior. Los síntomas en árboles afectados son el decaimiento en general del árbol, brotaciones poco vigorosas y pudrición de la médula y el duramen de las ramas. En varios años llega a la zona del tronco y provoca un decaimiento tan grande del árbol, que los frutos no llegan a ser comerciales como consecuencia de no terminar su proceso de crecimiento y maduración. Cuando se observan los carpoforos (setas) del hongo en el exterior, tal como se observa en las fotos, las caries en el interior están muy avanzadas y requeriría grandes cortes de saneamiento que además de costosas en muchos casos, no logran recuperar la productividad del frutal.
Estas enfermedades se caracterizan por la podredumbre de la madera, la cual pierde densidad y adquiere diversas coloraciones según los procesos enzimáticos involucrados en la desintegración:
* Podredumbres castañas o pardas: los hongos que las causan producen enzimas que degradan la celulosa y hemicelulosa, pero no afectan la lignina. Generalmente atacan árboles de madera blanda.
* Podredumbres blancas: Los hongos responsables de estas enfermedades producen, además de las mencionadas anteriormente, enzimas lignolíticas. Los árboles de madera dura, generalmente resistentes a los anteriores, son atacados por estos hongos.
.
.
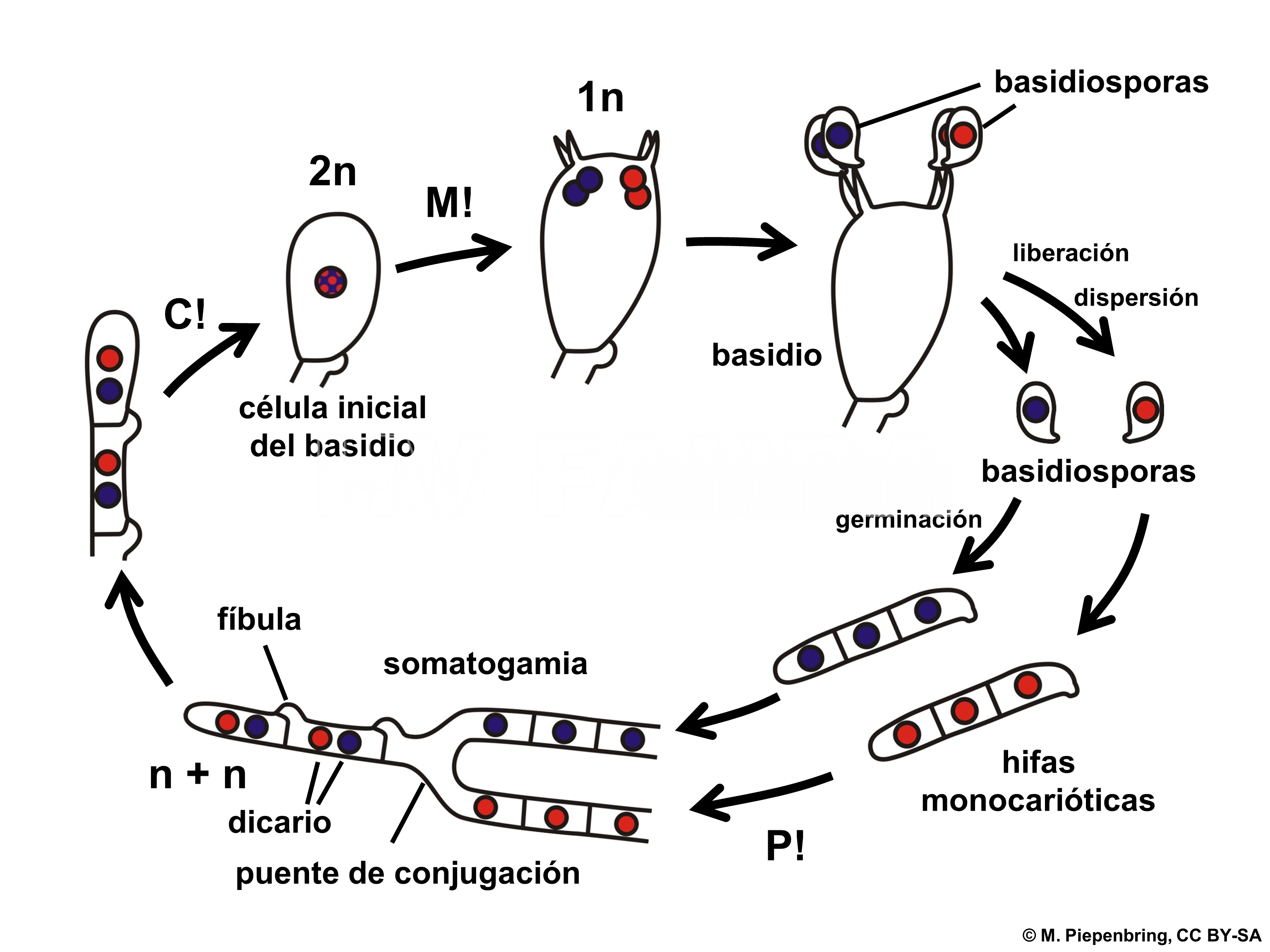
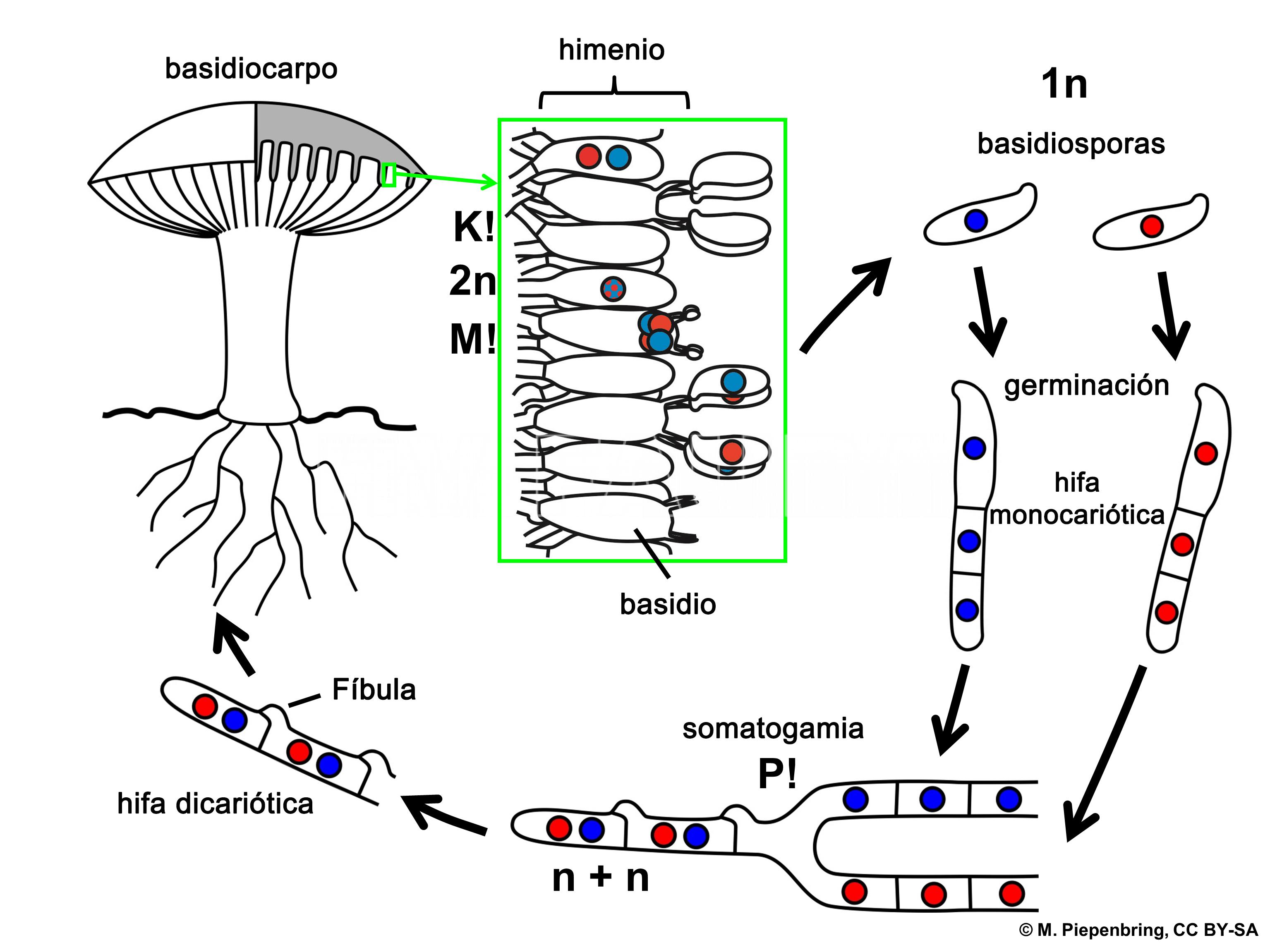
Ciclo de vida
Estas enfermedades se caracterizan por poseer un prolongado período de latencia, que puede ser incluso de años. Son consideradas enfermedades crónicas.
.
- Representación esquemática del ciclo de una carie de los árboles,. P! = plasmogamia; C! = cariogamia; M! = meiosis; 2n = células diploides; 1n = células haploides; n + n = células dicarióticas.
- Representación esquemática del ciclo de una carie de los árboles,. P! = plasmogamia; K! = cariogamia; M! = meiosis; 2n = células diploides; 1n = células haploides; n + n = células dicarióticas.
- Representación esquemática de Fíbulas. Luego de producida la plasmogamia el estado binucleado se mantiene por división conjugada de núcleos y posterior migración de los nuevos núcleos a través de fíbulas: proyecciones en forma de puente que conectan una célula hifal con otra.
- Hifas de basidiomycete con fíbula o unión en «abrazaderas» (clamps). Autor: Eivind Kverme Ronold
.
Manejo de la enfermedad
Puede ejercerse cierto control saneando las zonas de rotura de ramas, podando y eliminando hasta cerca del tronco las ramas rotas para impedir la infección; y sobre todo, con un buen manejo de la poda, ajustando la dirección del corte y evitando que el agua duerma en las heridas de poda, que éstas sean lo mas pequeñas posibles y utilizando productos para la protección de los cortes. Para evitar la dispersión de la enfermedad es conveniente quemar la ramas cortadas con síntomas de caries.
En resumen:
➞ Realizar podas adecuadas, evitando cortes grandes.
➞ Proteger las heridas del árbol con mástic o productos específicos.
➞ Eliminación de ramas infectadas.
➞ Eliminación de árboles infectados.
.
- 01 Árbol de ciruelo con basidiocarpos (fructificaciones) de hongos causantes de las caries.
- 02 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 03 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 04 Árbol de ciruelo con basidiocarpos (fructificaciones) de hongos causantes de las caries.
- 05 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 06 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 07 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 08 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 09 Árbol de ciruelo con basidiocarpos (fructificaciones) de hongos causantes de las caries.
- 10 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
- 11 Fructificación (basidiocarpo) del hongo causante de las caries en árbol de ciruelo.
.
.
.
Videos
How Mushrooms Changed the World
.
Bibliografía
Anderson JB, Bruhn JN, Kasimer D (2018) Clonal evolution and genome stability in a 2500-year-old fungal individual. Proceedings of the Royal Society B. doi: 10.1098/rspb.2018.2233
Ann P-J, Chang T-T, Ko W-H (2002) Phellinus noxius Brown Root Rot of Fruit and Ornamental Trees in Taiwan. Plant Disease 86(8): 820-826. doi: 10.1094/PDIS.2002.86.8.820
Anothai J, Intara-anun S, Samlikamnoed P, et al. (2023) Understanding factors influencing growth and lignocellulosic enzyme of Ganoderma for developing integrated control strategies for basal stem rot disease in oil palm. Trop. plant pathol. 48: 154–162. doi: 10.1007/s40858-022-00551-8
Baumgartner K, Coetzee MP, Hoffmeister D (2011) Secrets of the subterranean pathosystem of Armillaria. Mol Plant Pathol. 12(6): 515-34. doi: 10.1111/j.1364-3703.2010.00693.x
Bieker D, Kehr R, Weber G, et al. (2010) Non-destructive monitoring of early stages of white rot by Trametes versicolor in Fraxinus excelsior. Ann. For. Sci. 67: 210. doi: 10.1051/forest/2009103
Brooks FE (2002) Brown root rot. The Plant Health Instructor. Updated 2013. doi: 10.1094/PHI-I-2002-0923-01
Chang TT (1995) Decline of nine tree species with brown root rot caused by Phellinus noxius in Taiwan. Plant Disease 79: 962-965.
Chang T (2003) Effect of Soil Moisture Content on the Survival of Ganoderma Species and Other Wood-Inhabiting Fungi. Plant Disease 87(10): 1201‐1204. doi: 10.1094/PDIS.2003.87.10.1201
Chung C-L, Huang S-Y, Huang Y-C, et al. (2015) The Genetic Structure of Phellinus noxius and Dissemination Pattern of Brown Root Rot Disease in Taiwan. PLoS ONE 10(10): e0139445. doi: 10.1371/journal.pone.0139445
Chung C-L, Lee TJ, Akiba M, et al. ( 2017) Comparative and population genomic landscape of Phellinus noxius: A hypervariable fungus causing root rot in trees. Molecular Ecology: 1–16. doi: 10.1111/mec.14359
Collins C, Hurley R, Almutlaqah N, et al. (2017) Proteomic Characterization of Armillaria mellea Reveals Oxidative Stress Response Mechanisms and Altered Secondary Metabolism Profiles. Microorganisms. 5(3): 60. doi: 10.3390/microorganisms5030060
Cui BK, Li HJ, Ji X, et al. (2019) Species diversity, taxonomy and phylogeny of Polyporaceae (Basidiomycota) in China. Fungal Diversity 97: 137–392. doi: 10.1007/s13225-019-00427-4
Darlis D, Jalloh MB, Chin CFS, et al. (2023) Exploring the potential of Bornean polypore fungi as biological control agents against pathogenic Ganoderma boninense causing basal stem rot in oil palm. Sci Rep 13: 10316. doi: 10.1038/s41598-023-37507-0
Dewdney M (2012) Ganoderma root rot. Citrus industry 37
Fischer M, González García V (2015) An annotated checklist of European basidiomycetes related to white rot of grapevine Vitis vinifera. Phytopathol. Mediterr. 54: 281-298. doi: 10.14601/Phytopathol_Mediterr-16293
Hiscox J, O’Leary J, Boddy L (2018) Fungus wars: basidiomycete battles in wood decay. Stud Mycol. 89: 117-124. doi: 10.1016/j.simyco.2018.02.003
Ingold CT (1992) The basidium: a spore-gun of precise range. The Mycologist 6(3): 111-113. doi: 10.1016/S0269-915X(09)80588-0
Kijpornyongpan T, Schwartz A, Yaguchi A, et al. (2022) Systems biology-guided understanding of white-rot fungi for biotechnological applications: A review. iScience 25: 104640. doi: 10.1016/j.isci.2022.104640
Kowalczyk JE, Peng M, Pawlowski M, et al. (2019) The White-Rot Basidiomycete Dichomitus squalens Shows Highly Specific Transcriptional Response to Lignocellulose-Related Aromatic Compounds. Front. Bioeng. Biotechnol. 7: 229. doi: 10.3389/fbioe.2019.00229
Kuhar F, Papinutti L (2014) Optimization of laccase production by two strains of Ganoderma lucidum using phenolic and metallic inducers. Revista Argentina de Microbiología 46(2):144–149. doi: 10.1016/S0325-7541(14)70063-X
Kumar M, Pandey A, Ezhumalai R, Shukla S (2022) Wood Decay by Fungi: Challenges and Prevention. In: Sundararaj, R. (eds) Science of Wood Degradation and its Protection. Springer, Singapore. doi: 10.1007/978-981-16-8797-6_2
Leriche-Grandchamp M, Flourat A, Shen H, et al. (2020) Inhibition of Phenolics Uptake by Ligninolytic Fungal Cells and Its Potential as a Tool for the Production of Lignin-Derived Aromatic Building Blocks. Journal of Fungi. 6(4):362. doi: 10.3390/jof6040362
Loyd AL, Barnes CW, Held BW, et al. (2018) Elucidating «lucidum»: Distinguishing the diverse laccate Ganoderma species of the United States. PLoS ONE 13(7): e0199738. doi: 10.1371/journal.pone.0199738
Loyd AL, Linder ER, Smith ME, et al. (2019) Cultural characterization and chlamydospore function of the Ganodermataceae present in the eastern United States. Mycologia. 111(1): 1‐12. doi: 10.1080/00275514.2018.1543509
Luangharn T, Karunarathna SC, Hyde KD, Chukeatirote E (2014) Optimal conditions of mycelia growth of Laetiporus sulphureus sensu lato. Mycology 5(4): 221-227. doi: 10.1080/21501203.2014.957361
Machado AS, Valadares F, Silva TF, Milagres AMF, Segato F and Ferraz A (2020) The Secretome of Phanerochaete chrysosporium and Trametes versicolor Grown in Microcrystalline Cellulose and Use of the Enzymes for Hydrolysis of Lignocellulosic Materials. Front. Bioeng. Biotechnol. 8:826. doi: 10.3389/fbioe.2020.00826
Mallett KI (1990) Host range and geographic distribution of Armillaria root rot pathogens in the Canadian prairie provinces. Canadian Journal of Forest Research 20(12): 1859-1863. doi: 10.1139/x90-249
Maluin FN, Mohd ZH, Nor Azah Y, et al. (2019) Enhanced fungicidal efficacy on Ganoderma boninense by simultaneous co-delivery of hexaconazole and dazomet from their chitosan nanoparticles. RSC Adv. 9: 27083. doi: 10.1039/C9RA05417K
Markakis EA, Kavroulakis N, Ntougias S, et al. (2017) Characterization of Fungi Associated With Wood Decay of Tree Species and Grapevine in Greece. Plant Dis. 101(11): 1929-1940. doi: 10.1094/PDIS-12-16-1761-RE
Maryam K, Daryaei MG, Torkaman J, et al. (2017) Natural decomposition of hornbeam wood decayed by the white rot fungus Trametes versicolor. Anais da Academia Brasileira de Ciências 89: 2647-2655. doi: 10.1590/0001-3765201720160714
Nagy LG, Vonk PJ, Kunzler M, et al. (2021) Lessons on fruiting body morphogenesis from genomes and transcriptomes of Agaricomycetes. bioRxiv 2021.12.09.471732; doi: doi: 10.1101/2021.12.09.471732
Nogales A, Aguirreolea J, Santa María E, et al. (2009) Response of mycorrhizal grapevine to Armillaria mellea inoculation: disease development and polyamines. Plant Soil 317: 177. doi: 10.1007/s11104-008-9799-6
Oghenekaro AO, Kovalchuk A, Raffaello T, et al. (2020) Genome sequencing of Rigidoporus microporus provides insights on genes important for wood decay, latex tolerance and interspecific fungal interactions. Sci Rep 10: 5250. doi: 10.1038/s41598-020-62150-4
Petchayo Tigang S, Tchotet Tchoumi JM, Roux J, et al. (2020) Armillaria root rot threatens Cameroon’s Penja pepper (Piper nigrum L.). Tropical Plant Pathology 45: 534–543. doi: 10.1007/s40858-020-00361-w
Rytioja J, Hildén K, Yuzon J, et al. (2014) Plant-polysaccharide-degrading enzymes from Basidiomycetes. Microbiol Mol Biol Rev. 78(4): 614-649. doi: 10.1128/MMBR.00035-14
Silva FB, Mazarotto EJ, Santos AF, Auer CG (2018) Caracterização morfofisiológica e patogênica de isolados de Armillaria na região Sul do Brasil. Summa Phytopathologica 44(1): 23-31. doi: 10.1590/0100-5405/175653
Suzuki H, MacDonald J, Syed K, et al. (2012) Comparative genomics of the white-rot fungi, Phanerochaete carnosa and P. chrysosporium, to elucidate the genetic basis of the distinct wood types they colonize. BMC Genomics 13: 444 (2012). doi: 10.1186/1471-2164-13-444
Toapanta-Alban CE, Ordoñez ME, Blanchette RA (2022) New Findings on the Biology and Ecology of the Ecuadorian Amazon Fungus Polyporus leprieurii var. yasuniensis. Journal of Fungi. 8(2): 203. doi: 10.3390/jof8020203
White CL (2010) The characterization of the basidiomycetes and other fungi associated with Esca of grapevines in south africa. Master Thesis, Stellenbosch University. Link
Whiteford R, Nurika I, Schiller T, Barker G (2021) The white-rot fungus, Phanerochaete chrysosporium, under combinatorial stress produces variable oil profiles following analysis of secondary metabolites. J Appl Microbiol. doi: 10.1111/jam.15013
Wingfield BD, Berger DK, Coetzee MPA, et al. (2022) Draft genome sequences of an Armillaria species from Zimbabwe, Ceratocystis colombiana, Elsinoë necatrix, Rosellinia necatrix, two genomes of Sclerotinia minor, short‑read genome assemblies and annotations of four Pyrenophora teres isolates from barley grass, and a long-read genome assembly of Cercospora zeina. IMA genome‑F17. IMA Fungus 13, 19. doi: 10.1186/s43008-022-00104-3
Wong MY, Govender NT, Ong CS (2019) RNA-seq data of Ganoderma boninense at axenic culture condition and under in planta pathogen-oil palm (Elaeis guineensis Jacq.) interaction. BMC Research Notes 12: 631. doi: 10.1186/s13104-019-4652-y
Yang ZL (2011) Molecular techniques revolutionize knowledge of basidiomycete evolution. Fungal Diversity 50: 47. doi: 10.1007/s13225-011-0121-1
Zhou S, Zhang X, Ma F, et al. (2021) Integrative Analysis of Selected Metabolites and the Fungal Transcriptome during the Developmental Cycle of Ganoderma lucidum Strain G0119 Correlates Lignocellulose Degradation with Carbohydrate and Triterpenoid Metabolism. Appl Environ Microbiol. 87(13): e0053321. doi: 10.1128/AEM.00533-21